Пфизерова мРНА вакцина против ЦОВИД-а поново је распламсала страст за коришћењем рибонуклеинске киселине (РНА) као терапеутске мете.Међутим, циљање РНК малим молекулима је изузетно изазовно.
РНК има само четири грађевна блока: аденин (А), цитозин (Ц), гванин (Г) и урацил (У) који замењује тимин (Т) који се налази у ДНК.Ово чини селективност лекова готово непремостивом препреком.Насупрот томе, постоје 22 природне аминокиселине које чине протеине, што објашњава зашто већина лекова који циљају протеине има релативно добру селективност.
Структура и функција РНК
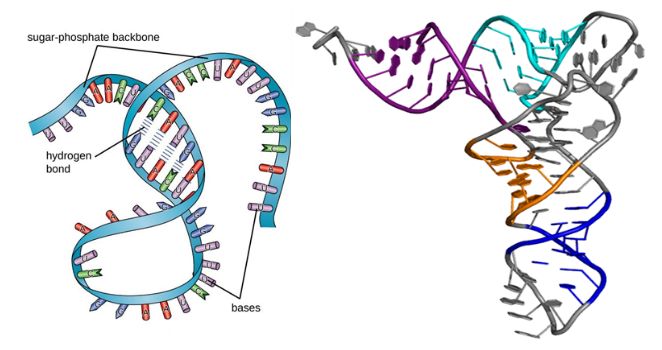
Као и протеини, молекули РНК имају секундарне и терцијарне структуре, као што је приказано на слици испод.Иако су једноланчани макромолекули, њихова секундарна структура добија облик када упаривање база узрокује избочине, петље и спирале.Затим, тродимензионално пресавијање доводи до терцијарне структуре РНК, која је неопходна за њену стабилност и функцију.
Слика 1. Структура РНК
Постоје три типа РНК:
- Месинџер РНК (мРНА)транскрибује генетске информације из ДНК и преноси се као базна секвенца на рибозом;л
- рибозомална РНК (рРНА)је део органела који синтетишу протеине званих рибозоми, који се извозе у цитоплазму и помажу у превођењу информација у мРНК у протеине;
- Трансфер РНК (тРНА)је веза између мРНК и ланца аминокиселина који чини протеин.
Циљање РНК као терапеутске мете је веома атрактивно.Утврђено је да је само 1,5% нашег генома на крају преведено у протеин, док се 70%-90% транскрибује у РНК.Молекули РНК су најважнији за све живе организме.Према „централној догми“ Френсиса Крика, најкритичнија улога РНК је да преведе генетске информације из ДНК у протеине.Осим тога, молекули РНК имају и друге функције, укључујући:
- Делују као адаптерски молекули у синтези протеина;л
- Служи као гласник између ДНК и рибозома;л
- Они су носиоци генетских информација у свим живим ћелијама;л
- Промовисање рибосомске селекције исправних аминокиселина, што је неопходно за синтезу нових протеинаин виво.
Антибиотици
Иако је откривен још 1940-их, механизам деловања многих антибиотика није разјашњен све до касних 1980-их.Утврђено је да велики део антибиотика делује тако што се везује за рибозоме бактерија како би их спречио да праве одговарајуће протеине, чиме убијају бактерије.
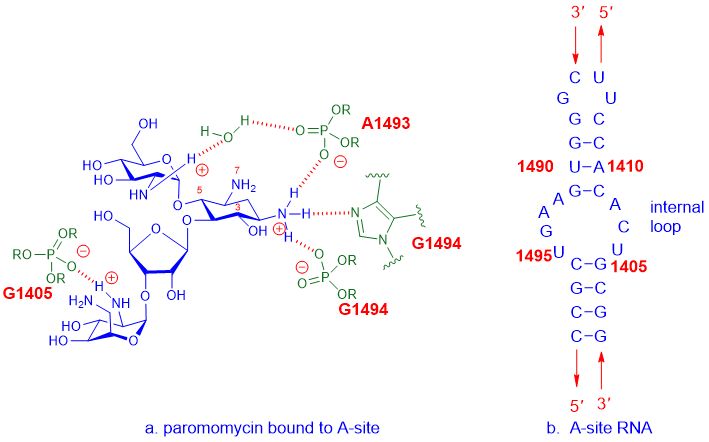
На пример, аминогликозидни антибиотици се везују за А-место 16С рРНА, која је део подјединице 30С рибозома, а затим ометају синтезу протеина да би ометали раст бактерија, што на крају доводи до смрти ћелије.А-место се односи на аминоацил место, такође познато као акцепторско место тРНК.Детаљна интеракција између аминогликозидних лекова, као нпрпаромомицин, и А-сајт офЕ. цолиРНК је приказана испод.
Слика 2. Интеракција између паромомицина и А-местаЕ. цолиРНА
Нажалост, многи инхибитори А-места, укључујући аминогликозидне лекове, имају безбедносне проблеме као што су нефротоксичност, доза зависна и специфична иреверзибилна ототоксичност.Ове токсичности су резултат недостатка селективности у аминогликозидним лековима за препознавање малих молекула РНК.
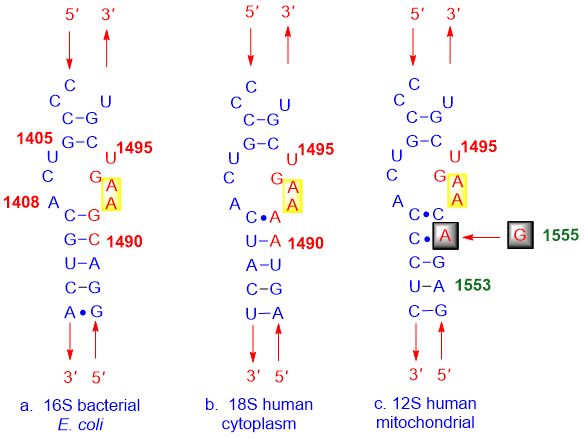
Као што је приказано на доњој слици: (а) структура бактерије, (б) мембрана људске ћелије и (ц) хумано митохондријално А-место су веома сличне, због чега се инхибитори А-места везују за све њих.
Слика 3. Везивање инхибитора неселективног А-места
Тетрациклински антибиотици такође инхибирају А-место рРНК.Они селективно инхибирају синтезу бактеријских протеина реверзибилним везивањем за спирални регион (Х34) на 30С подјединици у комплексу са Мг2+.
С друге стране, макролидни антибиотици се везују у близини излазног места (Е-места) бактеријског рибозомског тунела за настајуће пептиде (НПЕТ) и делимично га блокирају, чиме инхибирају синтезу бактеријског протеина.Коначно, оксазолидинон антибиотици као нпрлинезолид(Зивок) се везују за дубоки расцеп у бактеријској 50С рибозомској подјединици, која је окружена 23С рРНА нуклеотидима.
Антисенс олигонуклеотиди (АСО)
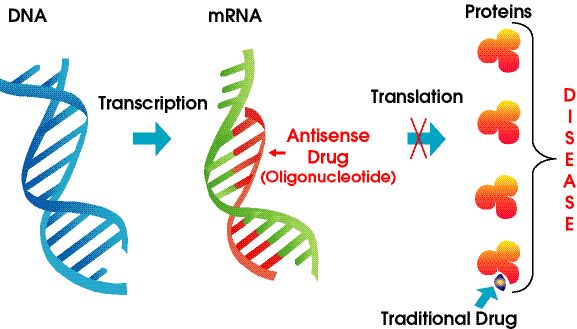
Антисенс лекови су хемијски модификовани полимери нуклеинских киселина који циљају РНК.Они се ослањају на упаривање Ватсон-Крикових база да се вежу за циљну мРНА, што доводи до утишавања гена, стеричне блокаде или измене спајања.АСО могу да интерагују са пре-РНК у ћелијском језгру и зрелим мРНК у цитоплазми.Они могу циљати егзоне, интроне и непреведене регионе (УТР).До данас је ФДА одобрила више десетина АСО лекова.
Слика 4. Антисенсе технологија
Лекови са малим молекулима који циљају РНК
Године 2015. Новартис је известио да су открили регулатор спајања СМН2 назван Бранаплам, који побољшава повезаност У1-пре-мРНА и спашава СМА мишеве.
С друге стране, ФДА је 2020. одобрила ПТЦ/Роцхеов Рисдиплам (Еврисди) за лечење СМА.Као и Бранаплам, Рисдиплам такође функционише тако што регулише спајање релевантних СМН2 гена за производњу функционалних СМН протеина.
РНК деградатори
РБМ је скраћеница за протеин мотива који се везује за РНК.У суштини, индол сулфонамид је молекуларни лепак.Он селективно регрутује РБМ39 у ЦРЛ4-ДЦАФ15 Е3 убиквитин лигазу, промовишући РБМ39 полиубиквитинацију и разградњу протеина.Генетско исцрпљивање или деградација РБМ39 посредована сулфонамидом изазива значајне абнормалности спајања у целом геному, што на крају доводи до смрти ћелије.
РНА-ПРОТАЦ-и су развијени да разграђују РНК-везујући протеини (РБП).ПРОТАЦ користи линкер да повеже лиганд Е3 лигазе са РНК лигандом, који се везује за РНК и РБП.Пошто РБП садржи структурне домене који се могу везати за специфичне олигонуклеотидне секвенце, РНА-ПРОТАЦ користи олигонуклеотидну секвенцу као лиганд за протеин од интереса (ПОИ).Коначни резултат је деградација РБП-а.
Недавно је професор Метју Дизни са Океанографског института Скрипс изумео РНКхимере које циљају рибонуклеазу (РибоТАЦ).РибоТАЦ је хетерофункционални молекул који повезује РНасе Л лиганд и РНК лиганд са линкером.Може специфично да регрутује ендогену РНКазу Л на специфичне РНК мете, а затим успешно елиминише РНК користећи механизам разградње ћелијске нуклеинске киселине (РНасе Л).
Како истраживачи сазнају више о интеракцији између малих молекула и РНК мета, у будућности ће се појавити више лекова који користе ову методу.
Време поста: 02.08.2023